不知不覺,斑馬魚已經在精準醫療上走了如此遠!
發布時間:
2018-05-02
斑馬魚模型在腫瘤領域的應用已經獲得了廣泛的認可,但是其在精確腫瘤學中的應用仍處于起步階段,目前來說還沒有直接使用斑馬魚來指導臨床患者治療特異性癌癥的案例。然而,相信在不久的將來,這個目標會得到實現。
其實,經由誘變、轉基因和異種移植的經典癌癥模型已經在精密腫瘤學的許多方面作出貢獻(圖1,左),但是斑馬魚癌癥模型的出現可以促進了(i)腫瘤發生和轉移中參與分子的鑒定和體內驗證;(ii)可行性改變和治療靶標的定義;(iii)發現腫瘤生物標志物和遺傳特征作為潛在的診斷和預后指標。
此外,一些研究已經證明了(iv)利用斑馬魚作為體內藥物篩選平臺鑒定和測試用于靶向抑制特定途徑/改變的藥物來更精確和直接地對精確腫瘤學作出貢獻的潛力。通過這種方法已經確定了許多可能代表個體化藥物的新型靶向藥物的小分子。
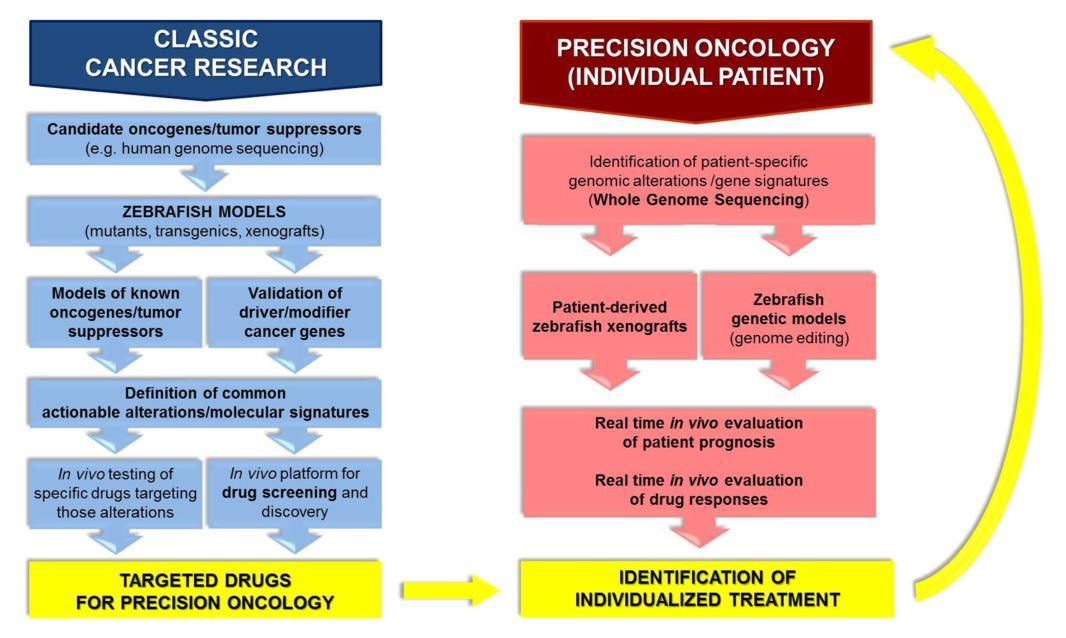
值得注意的是,迅速增加的患者也將斑馬魚推入了治療個體癌癥患者的臨床應用的道路上。各種研究已經證實這些模型在(v)體內評估患者預后中的適用性,以及(vi)基于對患者癌細胞異種移植物藥物的反應可以進行實時指導和個體化治療(圖1,右)。
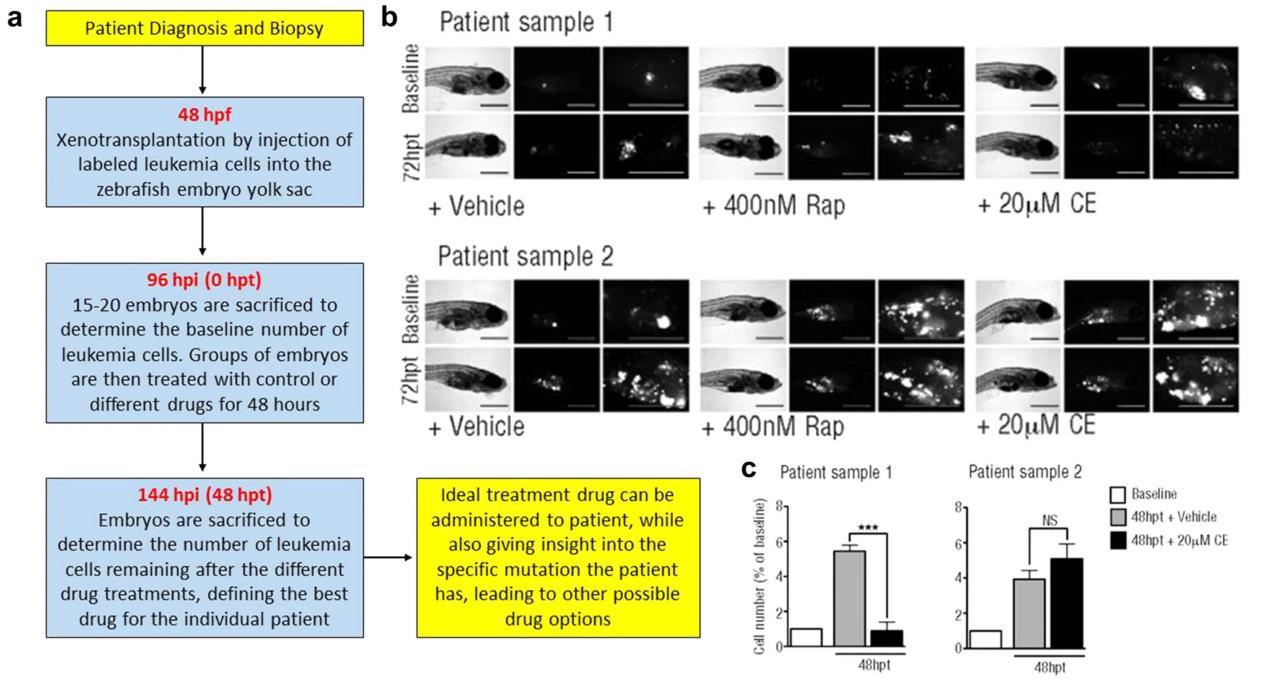
斑馬魚中癌癥的建模為精確腫瘤學的發展提供了重要的見解,也為直接臨床應用的優勢和可行性提供了直接的例子(圖2)。
迄今為止,已經有了無數的斑馬魚癌癥遺傳模型,并且數量繼續迅速持續增加著。已經使用多種策略開發了遺傳癌癥模型,包括瞬時、穩定和雙重轉基因以及各種誘變誘導劑(表2)并向著精準腫瘤學領域的應用前進。

自2005年起,人類細胞異種移植到斑馬魚上一直處于技術前沿,而該領域已經得到了迅速發展,利用各種注射部位、發育階段和移植標本(即人細胞系、患者衍生的原發性癌細胞、患者衍生的腫瘤組織外植體)的異種移植斑馬魚模型(表3)。斑馬魚移植模型提供了研究癌癥的許多標志和癌癥進展的步驟(例如自我更新、腫瘤誘導的血管生成、侵襲和傳播、腫瘤與宿主之間的相互作用以及藥物反應)的可能性。
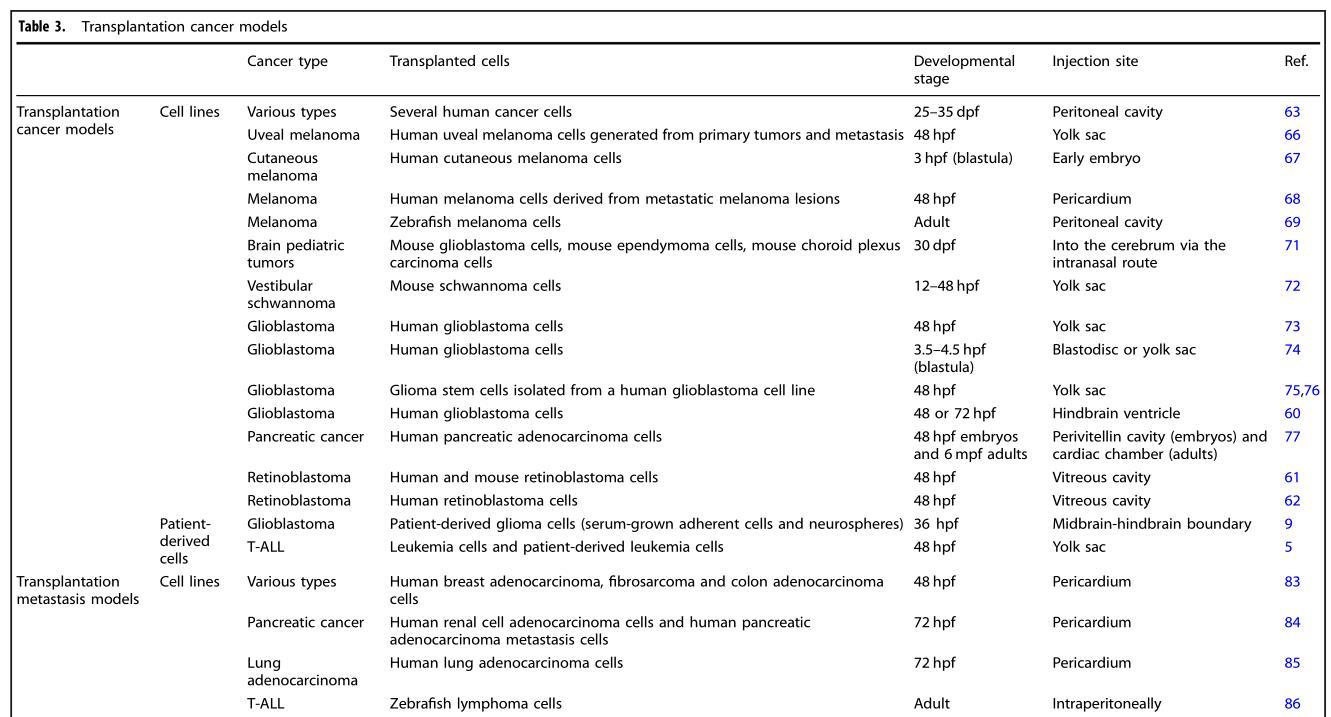
舉幾個近幾年出現的有關斑馬魚轉移模型的杰出例子(表3)。Stoletov et al.利用實時活體成像技術在48 hpf的斑馬魚胚胎的心包內注入熒光的人類癌細胞借以觀察血管內運動和外滲的動態過程,從而為涉及β1整合素、Twist和VEGFA的潛在分子調節過程提供新的見解。
Matteo et al.通過修改Stoletov的模型來證明神經氈蛋白-2通過與內皮α5整合素相互作用能促進人類胰腺癌和腎細胞癌細胞在斑馬魚中的外滲和轉移(圖3)。同時證明了斑馬魚外滲模型與哺乳動物轉移模型的協同作用,同時也表現出神經氈蛋白-2在小鼠中的轉移潛能(圖3)。因此,斑馬魚轉移模型可以作為驗證和支持鼠轉移數據的優秀體內平臺,反之亦然。

研究證明,斑馬魚轉移模型已經成為一個有希望的、并且在個性化醫療中的應用是可繼續發展的系統。繼續開發這些斑馬魚轉移模型,以及建立新的基于斑馬魚的精準醫療治療系統,將加速其在精密腫瘤學應用中的實施。